نظرة سريعة
يقدم هذا المقال دليلاً طبياً شاملاً لفهم “ارتفاع بيليروبين الدم” (اليرقان). نستعرض بدقة الفروقات بين يرقان البالغين وحديثي الولادة، وكيفية التمييز بين الحالات الفسيولوجية العابرة والمؤشرات المرضية الخطيرة كاليرقان النووي وانسداد القنوات الصفراوية. ستجد شرحاً لآليات التشخيص الحديثة، وتفسير الأعراض، وبروتوكولات العلاج المعتمدة عالمياً.
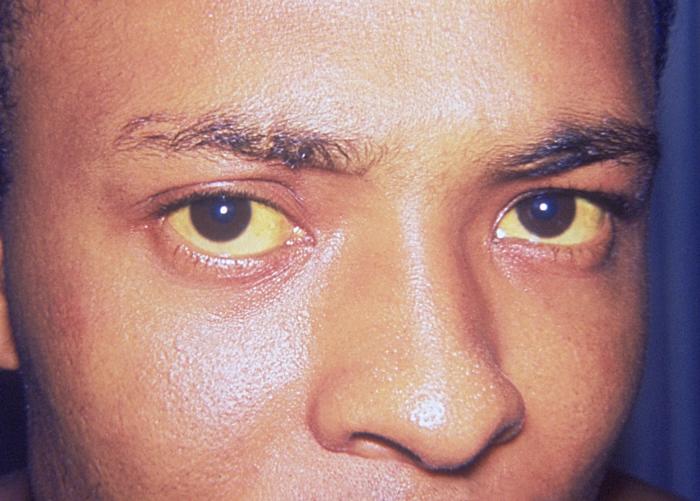
يحتل فرط بيليروبين الدم (Hyperbilirubinemia) حيزاً مهمًا في الممارسة الطبية اليومية، سواء في عيادات الأمراض الباطنية أو وحدات حديثي الولادة. وعلى الرغم من أن المظهر السريري المألوف لهذه الحالة يتمثل في اليرقان (Jaundice) – أي تلون الصلبة العينية والجلد والأغشية المخاطية باللون الأصفر – إلا أن الطبيب الممارس يدرك أن هذا العرض هو مجرد قمة جبل الجليد لاضطراب استقلابي كامن. يعكس اليرقان اختلالاً في التوازن الديناميكي بين معدل إنتاج البيليروبين وقدرة الكبد والجهاز الصفراوي على تصفية هذا المركب والتخلص منه.
بصفتي طبيباً أتعامل مع هذه الحالات، أجد أن التشخيص الدقيق يتطلب فهماً عميقاً للمسارات الكيميائية الحيوية للبيليروبين، حيث يُعد الارتفاع في مستويات البيليروبين المصلي (> 1.2 ملغم/ديسيلتر) علامة بيوكيميائية تستدعي تقييماً تشخيصياً صارماً لتحديد ما إذا كان الخلل يكمن في مرحلة ما قبل الكبد (انحلال الدم)، أو داخل الكبد (قصور خلوي)، أو ما بعد الكبد (انسداد ميكانيكي).
في هذه المقالة، سنستعرض بالتفصيل الآليات الفسيولوجية والمرضية، مع التركيز على أحدث الأدلة العلمية المنشورة حول التشخيص والعلاج.
فيزيولوجيا استقلاب البيليروبين (Bilirubin Metabolism)
لفهم المرض، يجب أولاً فهم المسار الفسيولوجي الطبيعي. يُعتبر البيليروبين المستقلب النهائي لعملية تكسر الهيم (Heme). تشير الدراسات إلى أن حوالي 80% من البيليروبين ينتج عن تكسر الهيموجلوبين في كريات الدم الحمراء الهرمة في الطحال، بينما تأتي الـ 20% الباقية من مصادر أخرى كالميوغلوبين وإنزيمات السيتوكروم. مصدر
تمر عملية الاستقلاب بثلاث مراحل معقدة:
- المرحلة قبل الكبدية (النقل): يتحلل الهيم بواسطة إنزيم “أكسيغناز الهيم” (Heme Oxygenase) إلى بيليفردين، والذي يُختزل فوراً إلى بيليروبين غير مقترن (Unconjugated Bilirubin). يتميز هذا المركب بكونه محباً للدهون (Lipophilic) وغير قابل للذوبان في الماء، مما يجعله ساماً للخلايا العصبية وقادراً على عبور الحاجز الدموي الدماغي. وللتنقل في الدم، يرتبط البيليروبين غير المقترن ببروتين الألبومين الذي يحمله إلى الكبد.
- المرحلة الكبدية (الاقتران – Conjugation): عند وصول المركب إلى الغشاء الجيبي للخلية الكبدية، ينفصل عن الألبومين وينتقل لداخل الخلية. هنا يحدث التفاعل الأهم: يقوم إنزيم (UGT1A1) بربط البيليروبين بحمض الغلوكورونيك، محولاً إياه إلى بيليروبين مقترن (Conjugated Bilirubin). هذا الشكل الجديد قابل للذوبان في الماء وغير سام، وهو الشكل الوحيد القابل للإفراز في العصارة الصفراوية.
- المرحلة ما بعد الكبدية (الإطراح): يُفرز البيليروبين المقترن عبر القنيات الصفراوية ليصل إلى الأمعاء. وهناك، تقوم البكتيريا المعوية بتحويله إلى مركبات عديمة اللون تسمى “يوروبيلينوجين”، والتي يتأكسد معظمها ليخرج مع البراز (ستيركوبيلين) معطياً إياه لونه البني، بينما يُعاد امتصاص جزء ضئيل ليدخل الدورة الدموية ويخرج عن طريق الكلى.
ارتفاع البيليروبين لدى البالغين
يُصنف اليرقان بناءً على موقع الخلل في مسار الاستقلاب. هذا التصنيف ليس أكاديمياً فحسب، بل هو الأساس الذي تُبنى عليه الخطة العلاجية.
1. اليرقان الانحلالي (Hemolytic Jaundice)
ينشأ هذا النوع عندما يتجاوز معدل تكسر كريات الدم الحمراء القدرة الاستيعابية للكبد على الاقتران. في هذه الحالة، يفيض البيليروبين غير المقترن في الدم.
- المسببات: تشمل فقر الدم المنجلي (Sickle Cell Anemia)، الثلاسيميا، نقص إنزيم G6PD (أنيميا الفول)، أو انحلال الدم المناعي الذاتي.
- المميزات السريرية: يظهر المريض بلون أصفر شاحب (ليموني)، وغالباً ما يكون البول والبراز بلون طبيعي (لأن البيليروبين غير المقترن لا يمر عبر الكلى). التحاليل تُظهر ارتفاعاً في البيليروبين غير المباشر، وارتفاع إنزيم LDH وانخفاض الهابتوجلوبين. مصدر
2. اليرقان الخلوي الكبدي (Hepatocellular Jaundice)
يحدث نتيجة ضرر مباشر في نسيج الكبد (Parenchyma) يعيق قدرة الخلايا على التقاط البيليروبين أو اقترانه.
- المسببات: التهابات الكبد الفيروسية (A, B, C)، تليف الكبد الكحولي أو الدهني، والسمية الدوائية (مثل الجرعات العالية من الأسيتامينوفين).
- متلازمة جيلبرت (Gilbert Syndrome): حالة وراثية حميدة شائعة جداً (تؤثر على 5-10% من السكان)، ناتجة عن طفرة في الجين المروج لإنزيم UGT1A1، مما يقلل من كفاءة الاقتران. يكون كبد المريض سليمًا تماماً، لكنه يعاني من ارتفاع طفيف في البيليروبين غير المقترن عند الصيام أو التوتر. تشير الدراسات الحديثة إلى أن هذه المتلازمة قد تحمل تأثيراً وقائياً ضد أمراض القلب والأوعية الدموية بفضل الخصائص المضادة للأكسدة للبيليروبين. مصدر
3. اليرقان الانسدادي (Obstructive/Cholestatic Jaundice)
ينتج عن إعاقة ميكانيكية تمنع تدفق الصفراء من الكبد إلى الأمعاء، مما يؤدي لارتجاع البيليروبين المقترن إلى الدم.
- المسببات: حصوات القناة الصفراوية الجامعة (Choledocholithiasis) هي السبب الأكثر شيوعاً. الأسباب الأخرى تشمل أورام رأس البنكرياس، سرطان الأقنية الصفراوية، أو تضيقات القنوات بعد الجراحة.
- المميزات السريرية: العلامة المميزة هي البول الداكن لأن البيليروبين المقترن يذوب في الماء ويخرج عبر الكلى، والبراز الشاحب (Acholic stool) لغياب الصبغة في الأمعاء، بالإضافة إلى حكة بالجلد. مخبرياً، ترتفع إنزيمات ALP وGGT بشكل ملحوظ.
ارتفاع بيليروبين الدم عند حديثي الولادة (Neonatal Hyperbilirubinemia)
تمثل هذه الفئة التحدي الأكبر في طب الأطفال، نظراً لخطورة السمية العصبية للبيليروبين.
1. اليرقان الفسيولوجي (Physiological Jaundice)
يحدث لدى 60% من المواليد الأصحاء. السبب هو “عدم نضج” فسيولوجي؛ حيث يكون عمر كريات الدم الحمراء للجنين قصيراً (مما يزيد إنتاج البيليروبين)، بينما يكون الكبد غير ناضج وغير قادر على إنتاج إنزيمات الاقتران بالسرعة الكافية. يظهر عادة في اليوم 2-3 بعد الولادة، ويبلغ ذروته في اليوم 4-5، ثم يتلاشى تلقائياً.
2. اليرقان المرضي واليرقان النووي (Kernicterus)
يعتبر اليرقان مرضياً إذا ظهر في أول 24 ساعة، أو ارتفع بمعدل سريع (> 0.5 ملغم/ديسيلتر/ساعة). السبب الأخطر هو انحلال الدم المناعي (عدم توافق فصائل الدم ABO أو Rh). الخطر الحقيقي يكمن في اليرقان النووي: إذا ارتفع البيليروبين غير المقترن لمستويات حرجة، فإنه يعبر الحاجز الدموي الدماغي ويترسب في العقد القاعدية (Basal Ganglia) وجذع الدماغ، مسبباً موتاً خلوياً (Apoptosis). تشير الأبحاث إلى أن هذا التلف يؤدي إلى شلل دماغي، صمم حسي عصبي، واضطرابات حركية دائمة، وهو ما يجعل الالتزام ببروتوكولات الفحص أمراً في غاية الأهمية. مصدر
3. توصيات الأكاديمية الأمريكية لطب الأطفال (AAP 2022)
أصدرت الأكاديمية تحديثاً شاملاً لإرشاداتها السريرية في 2022، مؤكدة على ضرورة:
- قياس البيليروبين (عن طريق الجلد أو المصل) لجميع المواليد قبل الخروج من المستشفى.
- استخدام الرسوم البيانية (Nomograms) المحدثة لتحديد عتبة العلاج الضوئي بناءً على عمر الحمل وساعات العمر وتواجد عوامل الخطر (مثل انحلال الدم). مصدر
البروتوكولات العلاجية الحديثة
لا يوجد علاج دوائي مباشر لخفض البيليروبين (مثل خافضات الحرارة)، بل يعتمد التدخل على معالجة السبب الجذري أو استخدام فيزياء الضوء.
1. العلاج الضوئي (Phototherapy): الآلية والتطبيق
هو العلاج الأساسي ليرقان المواليد. يعتمد مبدأه على تعريض جلد الطفل لضوء بطول موجي محدد (460-490 نانومتر – الطيف الأزرق). يقوم هذا الضوء بإحداث تفاعل كيميائي ضوئي يُعرف بـ التماكب الضوئي (Photoisomerization)، حيث يتحول جزيء البيليروبين السام (Z,Z-bilirubin) إلى متماكبات فراغية (Lumirubin) قابلة للذوبان في الماء، مما يسمح للجسم بإخراجها عبر الصفراء والبول دون الحاجة لعملية الاقتران الكبدي. تؤكد الدراسات أن فعالية العلاج تعتمد على “الجرعة الضوئية” (Irradiance) ومساحة سطح الجسم المعرضة للضوء. مصدر
2. تبديل الدم (Exchange Transfusion)
يُستخدم كحل إنقاذي أخير في حالات انحلال الدم الشديد المهدد لليرقان النووي، حيث يتم سحب دم الطفل المحمل بالبيليروبين والأجسام المضادة واستبداله بدم متبرع سليم.
3. التدخلات عند البالغين
- تصوير البنكرياس والقنوات الصفراوية بالمنظار (ERCP): هو الإجراء المفضل لاستخراج حصوات القناة الجامعة، حيث يجمع بين التشخيص والعلاج بتوسيع عضلة “أودي” وسحب الحصوات.
- الجراحة: استئصال المرارة (Cholecystectomy) هو الحل الجذري لمنع تكرار الحصوات.
- العلاجات الدوائية: استخدام حمض أورسوديوكسيكوليك (Ursodeoxycholic acid) في بعض حالات الركود الصفراوي المزمن لتحسين تدفق الصفراء.
الخلاصة
يعد فرط بيليروبين الدم مؤشراً سريرياً يتطلب مقاربة تشخيصية منهجية. مع أن معظم حالات يرقان المواليد (الفسيولوجي) ويرقان البالغين (جيلبرت) حميدة ولا تتطلب سوى المتابعة، فإن التمييز المبكر للحالات المرضية – كاليرقان الانسدادي أو الانحلالي – هو العامل الأهم في الوقاية من المضاعفات الخطيرة كالفشل الكبدي أو التلف الدماغي الدائم.
قائمة المصادر (References)
مصدر Maisels MJ, McDonagh AF. Phototherapy for Neonatal Jaundice. New England Journal of Medicine. 2008 Feb 28;358(9):920-8.
مصدر Kalakonda A, Jenkins BA, John S. Physiology, Bilirubin. StatPearls Publishing; 2024.
مصدر Norton J. Greenberger. Approach to the Patient with Jaundice. Current Diagnosis & Treatment. McGraw Hill; 2022.
مصدر Fargo MV, et al. Evaluation of Jaundice in Adults. American Family Physician. 2017 Feb 1;95(3):164-168.
مصدر Kemper AR, et al. Clinical Practice Guideline Revision: Management of Hyperbilirubinemia in the Newborn Infant. Pediatrics. 2022.
- الآثار الجانبية لحقن فيتامين د وأهم التحذيرات - 14 مارس، 2026
- كيف تؤثر أنظمة الحماية الذكية على الصحة النفسية؟ - 11 مارس، 2026
- بيئة المنزل والوقاية من الحساسية: دليل طبي لتحسين جودة الهواء - 11 مارس، 2026